G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,796
- Solutions
- 3
- Reaction score
- 3,063
- Points
- 113
- Deals
- 1
Sissejuhatus
Lüserghapet, emajuure alkaloididest saadud põhifragmenti, on sünteesitud neljateistkümnes järjestuses, alustades 3-beta-karboksüetüülindooliga. Lähtematerjal muudeti 1-bensoüül-5-keto-1,2,2a-3,4,5-heksahüdrobenz-[cd]-indooliks (3), mis sisaldab kolme lüserghappes esinevatest neljast rõngast. See ketoon omakorda muundati tetratsükliliseks ühendiks 9-keto-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo-[4,3-fe]-kinoliiniks (8) ja sealt edasi lüserghappeks (14). See süntees ei ole lihtne ja nõuab palju laboratoorset kogemust ja keemiateadmisi. Peale selle on mitmeid manipulatsioone ohtlike ainetega, mida tuleb teha rangete ohutusmeetmetega.
Keemistemperatuur: 536,2 ± 50,0 °C 760 mm Hg juures;
Sulamistemperatuur: 240 °C;
Molekulmass: 268,31 g/mool;
Tihedus: 1,4 ± 0,1 g/ml;
CASi number: 82-58-6.
Seadmed ja klaastooted:
- Terasest hüdrogeenimisreaktor 2-3 L;
- Terasest autoklaav 500 ml;
- Labori skaala (sobib 0,01 - 500 g);
- Ümarpõhjalised kolvid 100, 200, 500 ml, 5 ja 10 l;
- Vesiniku (H2) kompressor ja päritolu;
- Buchneri kolb ja lehter (suur) 5 L [väikeste koguste puhul võib kasutada Schott'i filtrit];
- Rotovap masin (suur);
- Vaakumallikas;
- 500 ml ja 2 L eraldussõnnikud;
- Lämmastikballoon ~50-70 L (1 baar);
- Kolbide septumkorgid;
- Soolane jääveevann;
- 5 L x2, 2 L x2; 1 L x2; 500 ml x2; 100 ml x3; 50 ml x2 keeduklaasid;
- Klaasist süstel või Pasteuri pipett;
- Magnetiline segisti või segisti;
- Vaakumdestillatsiooni seadeldis;
- tagasivoolukondensaator;
- Retordialus ja klamber aparatuuri kinnitamiseks;
- Laboratooriumitermomeeter (-20 °C kuni 200 °C) koos kolviadapteriga;
- pH-indikaatorpaber;
- Klaasvarda ja spaatel;
- 250 vatine lambipirn.
Reaktiivid.
- 3-Indolepropioonhape (1), 94,6 g (0,5 mol);
- 9,5 l destilleeritud vesi (H2O);
- ~ 400 g naatriumhüdroksiidi (NaOH);
- 116 g Raney-nikkel (Ni);
- 1050 ml soolhappe (HCl) kontsentreeritud;
- 2 ml väävelhapet (H2SO4 kontsentreeritud);
- 210 ml 12N naatriumhüdroksiidi (NaOH) vesilahust;
- 180 ml bensoüülkloriidi;
- ~1,5 L metanooli (MeOH);
- ~1,6 L etanooli (EtOH);
- 201,2 mL tionüülkloriidi (SOCl2);
- 1950 mL Süsinikdisulfiid (CS2);
- 240 g alumiiniumkloriidi (AlCl3);
- 2,5 L benseen;
- 500 ml 2N naatriumhüdroksiid (NaOH);
- ~3,2 L Dietüüleeter (Et2O);
- 3,3 L jäääädikhape (AcOH);
- 352 g (1,1 mol) püridiinhüdrobromiid-perbromiidi;
- 5 L kloroform (CHCl3);
- ~1000 g magneesiumsulfaati (MgSO4);
- 307 g (2,35 mol) metüülaminoatsetoon-etüleenketaal (5);
- 4,5 L benseen;
- ~500 g Aktiivsüsi (C);
- ~1 L atsetooni;
- ~500 g naatriumbikarbonaati (NaHCO3);
- 80 mL Külm äädikhappeanhüdriid (Ac2O);
- 1,5 g naatriumboorhüdriidi (NaBH4);
- 75 ml vääveldioksiidi (SO2 vedelik);
- 40 g naatriumtsüaniidi (NaCN pulber);
- 300 ml vesiniktsüaniidi (HCN vedelik);
- 78 ml 1,5% kaaliumhüdroksiidi (KOH) vesilahust;
- 8,5 g hüdraaditud naatriumarsenaati;
- ~ 50 ml ksüleen;
- 100 ml ammooniumhüdroksiidi (NH4OH) lahjendatud lahust;
- 16,9 g naatriummetoksiidi (MeONa).
Menetlus
1-Bensoüül-3-(beeta-karboksüetüül)-2,3-dihüdroindool (2)3-Indolepropioonhape (1), 94,6 g (0,5 mol), lahustati 600 ml vees, mis sisaldas 20 g naatriumhüdroksiidi. Lahus segati umbes 100 g Raney-nikkelkatalüsaatoriga ja hüdrogeeniti temperatuuril RT 2-3 l terasest hüdrogeenimispommis rõhul 3000-4000 psi (207-276 bar) H2. Redutseerimine oli tavaliselt täielik 20-30 tunni jooksul, mille järel katalüsaator filtreeriti ja pesti vähese veega. Filtraadile lisati 85 ml kontsentreeritud HCl-hapet ja lahus jahutati. Kui redutseerimine oli mittetäielik, eraldus sel hetkel reageerimata indoolpropioonhape ja see eemaldati filtreerimise teel. Filtraat bensoüüliti seejärel tavalise Schotten-Baumanni protseduuri abil, kasutades 210 ml 12N naatriumhüdroksiidi ja 180 ml bensoüülkloriidi. Lahust hoiti kogu bensoüülimise ajal leeliselisena ja temperatuuri hoiti alla 40 °C, jahutades. Kui bensoüülkloriid oli täielikult reageerinud, jahutati segu ja hapestati 300 ml kontsentreeritud HCl-happega. Toorprodukt filtreeriti ja pesti veega, seejärel ekstraheeriti see 4 x 1 l kuuma veega, et eemaldada bensoehape. Kuum siirupitaoline toode (2) kristalliseeriti pärast veeekstrakti dekanteerimist mõnest mahust metanoolist; saagis 103 g (70 %), MP: 151-153 °C.
1-Bensoüül-5-keto-1,2,2a,3,4,5-heksahüdrobens[cd]-indool (3)
1-Bensoüül-3-(beeta-karboksüetüül)-2,3-dihüdroindool (2), 118 g (0,4 mol), segati 200 ml puhta tionüülkloriidiga. Lahus jäeti 30 minutiks seisma, seejärel soojendati seda 15-20 minutit õrnalt auruvannil. Üleliigne tionüülkloriid aurustati täielikult alla 30 °C vaakumis ning toorhappekloriid lahustati 200 ml süsinikdisulfiidis. Seejärel lisati happekloriidi lahus õhukese joana 5 l kolvis (HOOD!!!) sisalduvale 240 g alumiiniumkloriidi tugevalt segatud suspensioonile 1750 ml süsinikdisulfiidis. Kompleks eraldus ja segamine muutus raskeks. Segu kuumutati tagasilöögi all ja segati ühe tunni jooksul, et reaktsioon lõpule viia, mille järel lagundati see väga ettevaatlikult, lisades 500 g jääd, 250 mL conc. HCl-hapet ja 500 mL vett. Lagundamise ajal hoiti segamist ja jahutamist mõjutas süsinikdisulfiidi perioodiline destilleerimine vaakumis ning toode ekstraheeriti 2 l benseeniga. Ekstrakti pesti põhjalikult 500 ml 2N naatriumhüdroksiidiga kolmes osas ja seejärel veega. See kuivatati magneesiumsulfaadi kohal ja seejärel aurustati vaakumis väikese mahuni. Mitme mahu eetri aeglane lisamine põhjustas kollase ketooni (3 ) kristalliseerumise. See filtreeriti ja pesti eetriga; saagis 85,3 g (77 %), MP: 146-147 °C. Analüüsiks kristalliseeriti proov ümber benseeni eetrist.
1-Bensoüül-3-(beeta-karboksüetüül)-2,3-dihüdroindool (2), 118 g (0,4 mol), segati 200 ml puhta tionüülkloriidiga. Lahus jäeti 30 minutiks seisma, seejärel soojendati seda 15-20 minutit õrnalt auruvannil. Üleliigne tionüülkloriid aurustati täielikult alla 30 °C vaakumis ning toorhappekloriid lahustati 200 ml süsinikdisulfiidis. Seejärel lisati happekloriidi lahus õhukese joana 5 l kolvis (HOOD!!!) sisalduvale 240 g alumiiniumkloriidi tugevalt segatud suspensioonile 1750 ml süsinikdisulfiidis. Kompleks eraldus ja segamine muutus raskeks. Segu kuumutati tagasilöögi all ja segati ühe tunni jooksul, et reaktsioon lõpule viia, mille järel lagundati see väga ettevaatlikult, lisades 500 g jääd, 250 mL conc. HCl-hapet ja 500 mL vett. Lagundamise ajal hoiti segamist ja jahutamist mõjutas süsinikdisulfiidi perioodiline destilleerimine vaakumis ning toode ekstraheeriti 2 l benseeniga. Ekstrakti pesti põhjalikult 500 ml 2N naatriumhüdroksiidiga kolmes osas ja seejärel veega. See kuivatati magneesiumsulfaadi kohal ja seejärel aurustati vaakumis väikese mahuni. Mitme mahu eetri aeglane lisamine põhjustas kollase ketooni (3 ) kristalliseerumise. See filtreeriti ja pesti eetriga; saagis 85,3 g (77 %), MP: 146-147 °C. Analüüsiks kristalliseeriti proov ümber benseeni eetrist.
1-Benzoyl-4-bromo-5-keto-1,2,2a,3,4,5-hexahydrobenz-[cd]-indole (4)
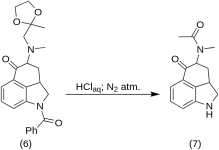
1-Bensoüül-2,2a,3,4-tetrahüdro-4-[metüül-(2-metüül-1,2-dioksolan-2-üülmetüül)-amino]-benz-[cd]-indool-5-(1H)-oon (6)
1-bensoüül-4-bromo-5-keto-1,2,2a,3,4,5-heksahüdrobenz-[cd]-indooli(4 ) 270 g (0,76 mol) ja 307 g (2.) lahus, mis on valmistatud 1-Bensoüül-4-bromo-5-keto-1,2,2a,3,4,5-heksahüdrobenz-[cd]-indooli(4) ja 307 g (2.) lahusest.35 mol) metüülaminoatsetoon-etüleenketaali (5 ) 4500 ml kuivas benseenis refluksiti lämmastiku all 21 tundi 10 l RBFis koos tagasivoolukondensaatoriga. Segu jahutati ja 151 g (93,5 %) metüülaminoatsetoon-etüleenketaalhüdrobromiidi filtreeriti, MP: 158-159 °C.
Filtraati pesti mitu korda jääveega, seejärel ekstraheeriti 2,5 l külma lahjendatud HCl-happega, mis sisaldas 150 ml kontsentreeritud hapet. Happeekstraktidele lisati kohe jääkülma lahjendatud naatriumhüdroksiidi ülejääk. Toode ekstraheeriti 1 L kloroformiga ning kloroformilahus kuivatati magneesiumsulfaadi kohal, töödeldi söega ja kontsentreeriti vaakumis. Ketaalketooni jääk (6 ) kristalliseeriti atsetoonist; MP: ja segu MP: 135-136 °C, saagis 220 g (71 %).
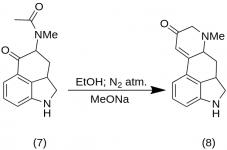
5-Keto-4-[N-metüül-N-atsetoonüülamino]-1,2,2a,3,4,5-heksahüdrobens[cd]-indool (7)
20 g 1-bensoüül-2,2a,3,4-tetrahüdro-4-[metüül-(2-metüül-1,3-dioksolan-2-üülmetüül)-amino]-benz-[cd]-indool-5-(1H)-oon (6 ) lahustati 250 mL kontsentreeritud HCl-happe ja 250 mL vee segus ning lahust hoiti lämmastiku all 37 °C juures 3-5 L RBFis viis päeva. Segu jahutati, töödeldi söega, filtreeriti ja filtraat kontsentreeriti vaakumis väikese mahuni. Jääki töödeldi liigse naatriumvesinikkarbonaadiga; toode ekstraheeriti külma kloroformiga ja lahusti eemaldati vaakumis temperatuuril RT. Toores diketoon (7 ) pulbristati, suspenseeriti umbes 75 ml 1:1 benseeni eetriga ja filtreeriti; saagis 9,8 g (77 %), MP: 105-107 °C. Analüüsitav proov kristalliseeriti ümber benseen-eetrist või etanoolist; MP: 109-110 °C; monohüdrokloriid saadi lahjendatud etanoolist; MP: 200 °C dets.
9-Keto-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo-[4,3-fg]-kinoliin (8)
25 g 5-Keto-4-[N-metüül-N-atsetoonüül]-amino-1,2,2a,3,4,5-heksahüdrobens[cd]-indooli (7 ) segati 550 ml absoluutse etanooliga. Segu segati lämmastiku all ja jahutati 2-5 l RBFis temperatuurini -15 °C. Seejärel lisati 16,9 g naatriummetoksiidi ja segu segati kümme minutit -10 °C kuni -12 °C juures. Reaktsioonisegu jahutati temperatuurini -25 °C ning toode filtreeriti 6,5-tollise buchneri lehtrile ning pesti vähese külma etanooli ja eetriga. Minimaalse kokkupuutega õhuga (sisaldab naatriummetoksiidi!) toorketoon (8 ) solgiti kohe vähese jääveega ja filtreeriti uuesti. Seda pesti jäävee, etanooli ja eetriga; saagis 16,2 g (69 %), MP: 145-147 °C. Analüütiline proov kristalliseeriti ümber lahjendatud etanoolist; MP: 155-157 °C; Dihüdrokloriid valmistati ja kristalliseeriti ümber vesialuselisest atsetoonist; MP: 270 °C dets.
4-atsetüül-9-keto-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliin (9)
9-keto-7-metüül-4,5,5a,6,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliin (8), 24 g, lisati 80 ml külma äädikhappeanhüdriidi. Segu hoiti 25 °C juures 200 mL RBFis umbes 5 minutit, seejärel jahutati see põhjalikult ning toode (9 ) filtreeriti ja pesti eetriga; saagis 20,5 g (76 %), mp: 167-170 °C. Filtraadi aurustamisel saadi teine saak; see suurendas kogusaagist 82%-ni. Üks proov kristalliseeriti ümber atsetoon-etanoolist; MP: 169-170 °C; hüdrokloriid valmistati etanoolis ja kristalliseeriti ümber vesialuselisest etanoolist; MP: 250 °C dets.
9-keto-7-metüül-4,5,5a,6,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliin (8), 24 g, lisati 80 ml külma äädikhappeanhüdriidi. Segu hoiti 25 °C juures 200 mL RBFis umbes 5 minutit, seejärel jahutati see põhjalikult ning toode (9 ) filtreeriti ja pesti eetriga; saagis 20,5 g (76 %), mp: 167-170 °C. Filtraadi aurustamisel saadi teine saak; see suurendas kogusaagist 82%-ni. Üks proov kristalliseeriti ümber atsetoon-etanoolist; MP: 169-170 °C; hüdrokloriid valmistati etanoolis ja kristalliseeriti ümber vesialuselisest etanoolist; MP: 250 °C dets.
4-atsetüül-9-hüdroksü-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliin (10)
10 g 4-atsetüül-9-keto-7-metüül-4,5,5,5a,6,6a,7,8,9-oktahüdroksindolo[4,3-fg]-kinoliini (9 ) lisati 150 mL metanooli ja 10 mL vee segule 500 mL RBFis. Lisati 1,5 g naatriumborohüdriidi ja lastakse reaktsioonil toimuda RT juures väikese mahuni ning lisatakse 15 mL conc. HCl-happe ja 60 mL vee segu. Jahutamisel eraldunud vesinikkloriid (10 ) filtreeriti ja pesti metanooliga, 9,0 g (79 %). Proov kristalliseeriti ümber lahjendatud etanoolist; MP: 245-246 °C dets.
4-Acetüül-9-kloro-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliinhüdrokloriid (11)
4-Acetüül-9-hüdroksü-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliinhüdrokloriid (10), 3.1 g, lahustati 75 ml vedelas vääveldioksiidis, mis oli klaasvooderdises 500 ml terasautoklaavis. Lisati tionüülkloriidi, 1,2 mL, ning anum suleti ja hoiti 25 °C juures 6 h. Autoklaav õhutati ja reaktsioonisegu eemaldati. Vääveldioksiidil lastakse aurustuda, samal ajal kui lahuse maht hoiti konstantsena kuiva eetri aeglase lisamisega. Amorfne klorohüdrokloriid (11 ) filtreeriti, pesti eetriga ja kuivatati vaakumis, MP: 130-135 °C dets. Saagis 3,5 g. 9-beta-epimeerilise alkoholi kasutamine selles reaktsioonis andis sama kloriidi võrreldava saagisega.
4-atsetüül-9-tsüano-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo-[4,3-fg]-kinoliin (12)
300 ml jääkülma vedela vesiniktsüaniidi juurde lisati 40 g kuiva, pulbristatud naatriumtsüaniidi. Segu segati ja jahutati jääl ning lisati 7,5 g eespool nimetatud toorest amorfset 4-atsetüül-9-kloro-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3f/g]-kinoliinhüdrokloriidi (11 ). Segamist jätkati 500 mL RBFis 30 min, mille järel vesiniktsüaniid destilleeriti kiiresti vähendatud rõhu all umbes 10 °C juures. Jääk segati kloroformi ja jääveega ning saadud segu filtreeriti. Orgaaniline kiht eraldati ja vesifaas ekstraheeriti kaks korda kloroformiga. Ühendatud ekstraktid kuivatati magneesiumsulfaadi kohal, värvitustamine lõpetati ja lahusti destilleeriti vaakumis. Toode (12 ) kristalliseeriti etüülatsetaadist; saagis 3,3 g (54% üle kogu alkoholi hüdrokloriidi põhjal), m.p. 172-174 °C. Ümberkristallisatsioon samast lahustist tõstis m.p. 181-182 °C-ni.
300 ml jääkülma vedela vesiniktsüaniidi juurde lisati 40 g kuiva, pulbristatud naatriumtsüaniidi. Segu segati ja jahutati jääl ning lisati 7,5 g eespool nimetatud toorest amorfset 4-atsetüül-9-kloro-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3f/g]-kinoliinhüdrokloriidi (11 ). Segamist jätkati 500 mL RBFis 30 min, mille järel vesiniktsüaniid destilleeriti kiiresti vähendatud rõhu all umbes 10 °C juures. Jääk segati kloroformi ja jääveega ning saadud segu filtreeriti. Orgaaniline kiht eraldati ja vesifaas ekstraheeriti kaks korda kloroformiga. Ühendatud ekstraktid kuivatati magneesiumsulfaadi kohal, värvitustamine lõpetati ja lahusti destilleeriti vaakumis. Toode (12 ) kristalliseeriti etüülatsetaadist; saagis 3,3 g (54% üle kogu alkoholi hüdrokloriidi põhjal), m.p. 172-174 °C. Ümberkristallisatsioon samast lahustist tõstis m.p. 181-182 °C-ni.
9-karbometoksü-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliin (13)
Eespool kirjeldatud toode (12 ), 1,0 g, segati 15 ml metanooli ja 0,25 ml veega. Segu jahutati ja lisati aeglaselt 2 ml kontsentreeritud väävelhapet. Lahus suleti klaastorusse lämmastiku all ja kuumutati 100 °C juures 23-24 tundi 100 mL RBFis koos tagasivoolukondensaatoriga. Segu töödeldi dekoloreeritud süsinikuga ja seejärel kontsentreeriti vaakumis umbes 10 mL-ni. See valati kloroformi (30 ml), jää ja 10 g naatriumbikarbonaadi segule. Kloroformi kiht eraldati ja vesifaas ekstraheeriti 3 x 10 mL kloroformiga. Ühendatud ekstraktid kuivatati magneesiumsulfaadi kohal, aurustati kuivaks ja toode (13 ) kristalliseeriti benseenist; saagis 0,51 g (53 %), MP: 159-160 °C. See kristalliseeriti ümber etüülatsetaadist; MP: 160-161 °C.
Eespool kirjeldatud toode (12 ), 1,0 g, segati 15 ml metanooli ja 0,25 ml veega. Segu jahutati ja lisati aeglaselt 2 ml kontsentreeritud väävelhapet. Lahus suleti klaastorusse lämmastiku all ja kuumutati 100 °C juures 23-24 tundi 100 mL RBFis koos tagasivoolukondensaatoriga. Segu töödeldi dekoloreeritud süsinikuga ja seejärel kontsentreeriti vaakumis umbes 10 mL-ni. See valati kloroformi (30 ml), jää ja 10 g naatriumbikarbonaadi segule. Kloroformi kiht eraldati ja vesifaas ekstraheeriti 3 x 10 mL kloroformiga. Ühendatud ekstraktid kuivatati magneesiumsulfaadi kohal, aurustati kuivaks ja toode (13 ) kristalliseeriti benseenist; saagis 0,51 g (53 %), MP: 159-160 °C. See kristalliseeriti ümber etüülatsetaadist; MP: 160-161 °C.
Sünteetiline dl-lüserghape (14)
9-karbometoksü-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliini (13), 3,9 g, ja 78 ml 1,5% kaaliumhüdroksiidi lahust refluksiti 30 minutit lämmastiku all. Lisati hüdreeritud naatriumarsenaat, 8,5 g, ja Raney-nikkel (16 g, märg), mis oli eelnevalt deaktiveeritud ksüleenisuspensioonis keetmise teel, ning segu kuumutati tagasivoolu all ja segati 20 tundi lämmastiku atmosfääris 200 mL RBFis koos tagasivoolukondensaatoriga. Lahust töödeldi süsinikuga ja toores lüserghape (14 ) sadestati neutraliseerimise teel pH-ni 5,6. See filtreeriti ja pesti veega; saagis 1,04 g, MP: 240-242 °C dets. saadi ka teine saak, 0,16 g, MP: 233-235 °C dets.; saagis kokku 30%. Hapet sai puhastada, lahustades seda lahjendatud ammooniumhüdroksiidis, töödeldes värvitust vähendava süsinikuga ja sadestades uuesti süsinikdioksiidiga, MP: 242-243 °C dets; segu looduslikust d-lüserghappest valmistatud dl-lüserghappega oli samuti 242-243 °C dets. Veevaba hapet saadi kuivatades vaakumis mitu tundi 150 °C juures.
9-karbometoksü-7-metüül-4,5,5a,6,6a,7,8,9-oktahüdroindolo[4,3-fg]-kinoliini (13), 3,9 g, ja 78 ml 1,5% kaaliumhüdroksiidi lahust refluksiti 30 minutit lämmastiku all. Lisati hüdreeritud naatriumarsenaat, 8,5 g, ja Raney-nikkel (16 g, märg), mis oli eelnevalt deaktiveeritud ksüleenisuspensioonis keetmise teel, ning segu kuumutati tagasivoolu all ja segati 20 tundi lämmastiku atmosfääris 200 mL RBFis koos tagasivoolukondensaatoriga. Lahust töödeldi süsinikuga ja toores lüserghape (14 ) sadestati neutraliseerimise teel pH-ni 5,6. See filtreeriti ja pesti veega; saagis 1,04 g, MP: 240-242 °C dets. saadi ka teine saak, 0,16 g, MP: 233-235 °C dets.; saagis kokku 30%. Hapet sai puhastada, lahustades seda lahjendatud ammooniumhüdroksiidis, töödeldes värvitust vähendava süsinikuga ja sadestades uuesti süsinikdioksiidiga, MP: 242-243 °C dets; segu looduslikust d-lüserghappest valmistatud dl-lüserghappega oli samuti 242-243 °C dets. Veevaba hapet saadi kuivatades vaakumis mitu tundi 150 °C juures.
Attachments
Last edited: